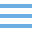燃料电池中通入燃料的一极为负极,通入氧气的一极为正极,燃料电池的反响原理相当于燃料的焚烧,据此书写电极反响式,并依据原电池中电子、离子的移动方向剖析回答;
(3)先依据电解池的作业原理确认阴、阳极,再依据阴、阳极的放电次序书写电极反响式,并剖析现象。
B.反响中H2别离生成LiNH2和LiH,LiNH2中H为+1价,LiH中H的化合价为-1价,则反响中H2既是氧化剂又是复原剂,故B正确;
C. Li+和H-的核外电子排布相同,Li+的核电核数更大,则半径更小,故C过错;
D.此法储氢是运用氧化复原反响将H2转化为固体资料,发生化学变化,而钢瓶储氢是将氢气液化,为物理变化,原理不同,故D过错;故答案为B;
(2)①设备B为氢氧燃料电池,通入氢气的电极为负极,通入氧气的电极为正极,电池作业时,电子从负极经过外电路流向正极,即从a极流向b极,电解质溶液中阳离子向正极移动,即H+由a极经过固体酸电解质传递到b极;
②b极为正极,发生复原反响,电极反响式为O2+4e-+4H+=2H2O;
(3)氢氧燃料电池中,a极为负极,b极为正极,则电解池中,X极为阴极,Y为阳极,
①X极为阴极,该电极上为水电离出的氢离子发生得电子的复原反响,一起生成氢氧根离子,即2H2O+2e-=H2↑+2OH-,溶液碱性增强,因而滴有酚酞的溶液变红;
②Y极为阳极,该电极上氯离子发生失电子的氧化反响,即2Cl--2e-=Cl2↑,产品为氯气,查验方法为用湿润的KI-淀粉试纸挨近Y极气体产品,试纸变蓝,证明发生Cl2。
![]()
【标题】某学习小组在试验室中运用下图设备(夹持设备省略)测定某铁硫化物(FexSy)的组成,并探求反响后D设备所得溶液中含硫化合物的组成。

进程Ⅲ当硬质玻璃管中固体质量不再改动时,中止加热,持续通入—段时刻的O2
(2)进程Ⅲ中,中止加热后还需持续通入一段时刻的O2,其意图为__________________。
(3)进程IV中制造溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有___________________。
(4)取25. 00 mL进程IV中所配溶液,参加足量的双氧水,再参加足量盐酸酸化的BaCl2溶液,将所得沉积过滤、洗刷、枯燥,称其质量为4.66g。则FexSy的化学式为___________________。
(5)问题评论:有同学以为可将设备D改为装有足量碱石灰的枯燥管,经过测定反响前后枯燥管的增重来核算硫元素的含量。你以为此计划________(填“是”或“否”)合理,原由于_______________________。
【标题】同温同压下,等体积的N2O和CO2两种气体相比较:①质量持平;②所含原子数持平;③所含电子数持平;④所含分子数持平;⑤所含氧原子数持平,上述定论中不正确的是()
某样品中含有碳酸钠及少数的硫酸钠和氯化钠。某学生为了查验其成分,依照下图所示进程进行试验,请将所加试剂及有关定论填写在相应的空格中。
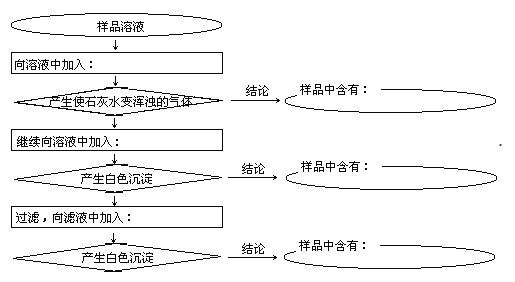
(3)向滤液2中先参加EDTA,再参加饱满Na2C03溶液,90℃充沛反响后,别离出固体Li2CO3粗品的操作是_______。
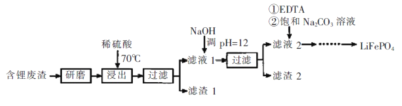
(5)将Li2CO3转化为LiHCO3后,用隔阂法电解LiHCO31溶液制备高纯度的LiOH,再转化得电池级Li2CO3。电解原理如图所示,阳极的电极反响式是____,该池运用了_________(填“阳”或“阴”)离子交换膜。
(6)将电池级Li2CO3和C、FePO4高温下反响,生成LiFePO4和一种可燃性气体,该反响的化学方程式是_________。
【标题】我国科学家运用双功用催化剂(能吸附不同粒子)催化水煤气改换反响:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH<0,在低温下取得高转化率与高反响速率。反响进程示意图如下:

从植物安排中获取挥发性成分。这些挥发性成分的混合物总称精油,大都具有令人愉快的香味。从柠檬、橙子和蜜柚等生果的果皮中提取的精油
![]()
②松开活塞K。加热水蒸气发生器至水欢腾,活塞K的支管口有很多水蒸气冒出时旋紧,翻开冷凝水,水蒸气蒸馏即开端做,可观察到在馏出液的水面上有一层很薄的油层。下列说法不正确的是